Valinomycin
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Valinomycin | ||||||||||||||||||
| Andere Namen | Cyclo(D-α-hydroxyisovaleryl-D-valyl-L-lactoyl-L-valyl-D-α-hydroxyisovaleryl-D-valyl-L-lactoyl-L-valyl-D-α-hydroxyisovaleryl-D-valyl-L-lactoyl-L-valyl) | ||||||||||||||||||
| Summenformel | C54H90N6O18 | ||||||||||||||||||
| Kurzbeschreibung | beigefarbener Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 1111,32 g·mol−1 | ||||||||||||||||||
| Aggregatzustand | fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit | nahezu unlöslich in Wasser[3] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Valinomycin ist ein Cyclodeca-Depsipeptid und zählt zu den Makrolid-Antibiotika. Es wird von mehreren Arten von Streptomyceten (z. B. Streptomyces fulvissimus) produziert.
Struktur
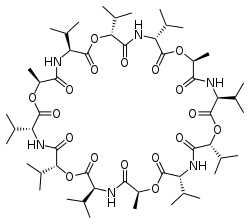
Valinomycin besteht aus den enantiomeren Aminosäuren L-Valin und D-Valin sowie den Hydroxysäuren L-Lactat und D-Hydroxyisovalerat. Die cyclische Struktur, bestehend aus der dreifach repetitiven Tetra-Depsipeptid-Einheit [–L-Lac–L-Val–D-Hiv–D-Val–]3, bildet einen symmetrischen Ring mit 36 Atomen aus wechselnden Amid- und Ester-Bindungen.
Eigenschaften
Valinomycin ist ein Ionophor, das selektiv Kalium-Ionen transportiert.[5][6] Dabei wird K+ in einer käfigartigen Struktur komplexiert und so durch die Zellmembran transportiert. Durch diese Transportvorgänge bricht das Membranpotential zusammen und die Zelle stirbt ab.[7]
Die Komplexbildungskonstante für den Kalium-Valinomycin-Komplex beträgt 106, während sie für den Natrium-Valinomycin-Komplex lediglich bei 10 liegt. Dieser große Unterschied (Selektivität) ist für die Transportvorgänge in biologischen Systemen von großer Wichtigkeit.
Verwendung
Die meisten Elektroden zum Nachweis von Kaliumionen nutzen die spezifische Komplexierung von Kaliumionen durch Valinomycin, welches in einer Konzentration von etwa 0,7 % in eine Kunststoffmembran eingebettet ist.
Weblinks
- The Virtual Museum of Minerals and Molecules: Valinomycin
Einzelnachweise
- ↑ Datenblatt Valinomycin bei Sigma-Aldrich, abgerufen am 25. April 2011 (PDF).
- ↑ a b Eintrag zu Valinomycin in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM) (Seite nicht mehr abrufbar)
- ↑ Eintrag zu Valinomycin. In: Römpp Online. Georg Thieme Verlag, abgerufen am 29. Dezember 2014.
- ↑ a b Eintrag zu Valinomycin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- ↑ Rose Lars und Jenkins ATA: The effect of the ionophore valinomycin on biomimetic solid supported lipid DPPTE/EPC membranes. In: Bioelectrochem. 70. Jahrgang, Nr. 2, 2007, S. 387–393, PMID 16875886.
- ↑ Cammann K: Ion-selective bulk membranes as models for biomembranes. In: Top. Curr. Chem. 128. Jahrgang, 1985, S. 219–258, doi:10.1007/3-540-15136-2_8.
- ↑ Safiulina D, Veksler V, Zharkovsky A und Kaasik A: Loss of mitochondrial membrane potential is associated with increase in mitochondrial volume: physiological role in neurones. In: J Cell Physiol. 206. Jahrgang, Nr. 2, 2006, S. 347–353, PMID 16110491.
Auf dieser Seite verwendete Medien
Chemical structure of valinomycin.
Global harmonisiertes System zur Einstufung und Kennzeichnung von Chemikalien (GHS): Piktogramm für giftige / toxische Chemikalien


