Tellurtetraiodid
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
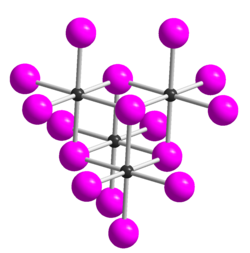 | |||||||||||||||||||
| _ Te4+ _ I− Te4I16-Einheit in der Kristallstruktur von TeI4 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Tellurtetraiodid | ||||||||||||||||||
| Andere Namen | Tellur(IV)-iodid | ||||||||||||||||||
| Verhältnisformel | TeI4 | ||||||||||||||||||
| Kurzbeschreibung | grauer bis schwarzer Feststoff mit beißendem Geruch[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 635,22 g·mol−1 | ||||||||||||||||||
| Aggregatzustand | fest[1] | ||||||||||||||||||
| Dichte | 5,403 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit | Zersetzung in Wasser[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Tellurtetraiodid ist eine anorganische chemische Verbindung des Tellurs aus der Gruppe der Iodide.
Gewinnung und Darstellung
Tellurtetraiodid kann durch Reaktion von Tellursäure mit Iodwasserstoff gewonnen werden.[2]
Es kann auch durch Reaktion von Tellur und Iod gewonnen werden, wobei je nach Reaktionsbedingungen auch Tellurdiiodid und Tellurmonoiodid entstehen können.[3]
Eigenschaften
Tellurtetraiodid ist ein eisengrauer Feststoff, der sich in kaltem Wasser langsam, in warmem Wasser rasch zu Tellurdioxid und Iodwasserstoff zersetzt.[1] Er ist beständig auch an feuchter Luft und zersetzt sich beim Erhitzen unter Iod-Abgabe. Er ist löslich in Iodwasserstoffsäure unter Bildung von H[TeI5] und etwas löslich in Aceton.[2] Von Tellurtetraiodid sind fünf Modifikationen bekannt, die alle aus tetrameren Molekülen aufgebaut sind.[4] Die δ-Form ist die thermodynamisch stabilste Form. Diese leitet sich (wie auch die α-,β- und γ-Form) strukturell von der ε-Form ab. Diese besitzt eine Struktur vom Kuban-Typ, die sich als aus vier über Halogenidbrücken verknüpften TeI3+I−-Einheiten zusammengesetzt beschreiben lässt. Die Formen unterscheiden sich dadurch, dass eine TeI3-Ecke des Würfels verschoben ist.[5]
Einzelnachweise
- ↑ a b c d e f g h Datenblatt Tellurium(IV) iodide, 99% (metals basis) bei Alfa Aesar, abgerufen am 17. Dezember 2013 (Seite nicht mehr abrufbar).
- ↑ a b Georg Brauer, unter Mitarbeit von Marianne Baudler u. a. (Hrsg.): Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band 1. Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 435.
- ↑ J. J. Zuckerman: Inorganic Reactions and Methods, The Formation of Bonds to Halogens. John Wiley & Sons, 2009, ISBN 0-470-14538-2, S. 59 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Erwin Riedel, Christoph Janiak: Anorganische Chemie. Walter de Gruyter, 2011, ISBN 3-11-022567-0, S. 461 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 101. Auflage. Walter de Gruyter, Berlin 1995, ISBN 3-11-012641-9, S. 632.
Auf dieser Seite verwendete Medien
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for corrosive substances
Global harmonisiertes System zur Einstufung und Kennzeichnung von Chemikalien (GHS): Piktogramm für giftige / toxische Chemikalien
Autor/Urheber: Andif1, Lizenz: CC BY-SA 4.0
Te4I16 unit in the crystal structure of TeI4. Created using Diamond 4. Data from Blackmore, W.R.; Abrahams, S.C.; Kalnajs, J. A Crystallographic Study of the Tellurium-Iodine System Acta Crystallographica (1,1948-23,1967), 9, 295-296 (1956)




