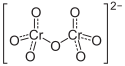
Rubidiumdichromat
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Rubidiumdichromat | |||||||||||||||
| Summenformel | Rb2Cr2O7 | |||||||||||||||
| Kurzbeschreibung | rote trikline oder gelbe monokline Kristalle[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 386,924 g·mol−1 | |||||||||||||||
| Aggregatzustand | fest | |||||||||||||||
| Dichte | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Rubidiumdichromat ist eine chemische Verbindung aus Rubidium, Chrom und Sauerstoff.
Gewinnung und Darstellung
Rubidiumdichromat kann durch Reaktion von Rubidiumcarbonat und Chrom(VI)-oxid[4]
oder Ammoniumdichromat mit Rubidiumchlorid gewonnen werden.[4]
Eigenschaften
Physikalische Eigenschaften
Rubidiumdichromat kommt in zwei verschiedenen Kristallstrukturen vor:
- Eine trikline Modifikation mit der Raumgruppe P1(Ci1), die die Gitterparameter a = 13,554 Å, b = 7,640 Å, c = 7,735 Å, α = 93,64°, β = 98,52°, und γ = 88,80° hat. In der Elementarzelle befinden sich 4 Formeleinheiten.[5]
- Eine monokline Modifikation mit der Raumgruppe P21/n.[6]
Chemische Eigenschaften
Rubidiumdichromat reagiert mit Chromtrioxid zu Rubidiumtetrachromat.[7]
Mit Rubidiumcarbonat bildet sich Rubidiumchromat.
Verwendung
Rubidiumdichromat wird zur Herstellung von elementarem Rubidium verwendet. Dazu wird es im Hochvakuum bei 500 °C mit Zirconium zur Reaktion gebracht:[8]
Einzelnachweise
- ↑ a b c Dale L. Perry, Sidney L. Phillips: Handbook of inorganic compounds. CRC Press, 1995, ISBN 978-0-8493-8671-8, S. 334 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Eintrag zu Chrom(VI)-verbindungen in der GESTIS-Stoffdatenbank des IFA, abgerufen am 10. Januar 2017. (JavaScript erforderlich)
- ↑ Nicht explizit in Verordnung (EG) Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag Chromium (VI) compounds, with the exception of barium chromate and of compounds specified elsewhere in this Annex in der Datenbank ECHA CHEM der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ a b Georg Brauer (Hrsg.) u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band III, Ferdinand Enke, Stuttgart 1981, ISBN 3-432-87823-0, S. 1526.
- ↑ N. Ch. Panagiotopoulos, I. D. Brown: Crystal structure of triclinic rubidium dichromate, Rb2Cr2O7. In: Canadian Journal of Chemistry. 48 (4), 1970, S. 537, doi:10.1139/v70-089.
- ↑ Robert L. Carter: "Comparison of the vibrational spectra of K2Cr2O7, Rb2Cr2O7 and Cs2Cr2O7" in Spectrochimica Acta A 1973, 29(2), S. 253–262. doi:10.1016/0584-8539(73)80069-8
- ↑ Percy Löfgren: "The crystal structure of rubidium tetrachromate, Rb2Cr4O13" in Acta Cryst. 1973, 29, S. 2141. doi:10.1107/S0567740873006242
- ↑ Mary Eagleson: Concise encyclopedia chemisry Berlin; New York: de Gruyter, 1994, ISBN 3-11-011451-8, S. 958 (eingeschränkte Vorschau in der Google-Buchsuche).
Auf dieser Seite verwendete Medien
Globales Harmonisiertes System zur Einstufung und Kennzeichnung von Chemikalien (GHS) Piktogramm für gesundheitsgefährdende Stoffe.
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for environmentally hazardous substances
Struktur des Rb+-Ions
Struktur des Dichromat-Ions
Die Zahl 2