Noradrenalin
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Norepinephrin | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C8H11NO3 | |||||||||||||||||||||
| Kurzbeschreibung | farblose Kristalle[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | C01CA03 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | ||||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit | in Wasser, Ethanol und Diethylether praktisch unlöslich[1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Noradrenalin (älter Nor-Adrenalin) oder Norepinephrin (INN), bekannt auch unter seinem Handelsnamen Arterenol, ist ein körpereigener Botenstoff, der als Stresshormon und Neurotransmitter wirkt. Als Körperhormon wird die Substanz im Nebennierenmark gebildet; als Neurotransmitter dagegen im Nervensystem produziert (im Locus caeruleus).
Noradrenalin ist ein Katecholamin und eng mit Adrenalin verwandt. Durch Verengung von Blutgefäßen erhöht es den Blutdruck. Wie die englische Vorsilbe Nor- anzeigt, trägt „Nor-Adrenalin“ („noch nicht“ Adrenalin[5]) im Vergleich zum Adrenalin keine Methylgruppe (-CH3) an seiner Aminogruppe. Daher zeigen Noradrenalin und Adrenalin zum Teil physiologisch unterschiedliche Wirkungen.
| Katecholamine (Vergleich) |
|---|
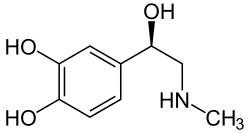 Adrenalin |
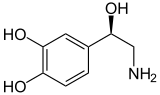 Noradrenalin |
Geschichte
Das Noradrenalin wurde um 1948 von Peter Holtz, der es zu dieser Zeit noch Norepinephrin nannte, sowie von Ulf von Euler[6] entdeckt. Durch diese Entdeckung konnte wenige Zeit später die physiologische Wirkung der beiden Nebennierenhormone (Noradrenalin und Adrenalin) geklärt werden. 1949 führte Marcel Goldenberg das Noradrenalin zur Therapie bei schwerem Schock ein.[7]
Wirkung als Hormon
Noradrenalin wird neben dem Adrenalin als Hormon in den Nebennieren produziert und ins Blut abgegeben (Fluchtreflex). Es wirkt vorwiegend an den Arteriolen und führt über Aktivierung von Adrenozeptoren zu einer Engstellung dieser Gefäße und damit zu einer Blutdrucksteigerung.
Wirkung als Neurotransmitter
Die wichtigste Funktion von Noradrenalin ist seine Rolle als Neurotransmitter im Zentralnervensystem und dem sympathischen Nervensystem. Damit unterscheidet sich Noradrenalin vom Adrenalin, welches nur eine untergeordnete Neurotransmitterrolle besitzt.[8]
Noradrenalin wird im peripheren Nervensystem von sympathischen Nervenfasern ausgeschüttet. Es ist eine Überträgersubstanz (Neurotransmitter) der postganglionären Synapsen des sympathischen Nervensystems und entfaltet dort weitgehend die gleiche Wirkung wie Adrenalin (aus dem Nebennierenmark). Die Eliminierung des Noradrenalins aus dem synaptischen Spalt erfolgt hauptsächlich durch Wiederaufnahme in die präsynaptische Zelle über den Transporter, kann aber auch enzymatisch inaktiviert werden. Noradrenalin-Wiederaufnahmehemmer führen zu einer Erhöhung der Noradrenalin-Konzentration und somit zu einer Erhöhung des Sympathikotonus.
Im Locus caeruleus, einer relativ kleinen, dunkelfarbigen Zellgruppe in der vorderen Rautengrube, einem Teil der Brücke (Pons), wird ein Großteil des Noradrenalins des ZNS produziert. Benzodiazepine vermindern die Aktivität des Locus caeruleus und reduzieren damit den Transport von Noradrenalin zum Vorderhirn.
Klinische Angaben
Biochemie
Noradrenalin gehört, wie beispielsweise auch Adrenalin und Dopamin, zur Gruppe der Katecholamine. Sein natürliches Stereoisomer ist L-(−)-Noradrenalin [Synonym: (R)-Noradrenalin], und dessen Enantiomer D-(+)-Noradrenalin [Synonym: (S)-Noradrenalin] ist physiologisch unbedeutend.
Die Produktion von Noradrenalin erfolgt in den Nebennieren und im Nervensystem aus Dopamin mittels des Enzyms Dopaminhydroxylase. Als Kofaktor und Elektronendonator spielt Vitamin C eine Rolle.[9]
Pathologische Relevanz
Eine pathologisch erhöhte Konzentration an Noradrenalin im Blut findet sich beim Krankheitsbild der Herzinsuffizienz.
Anwendung als Arzneistoff
Noradrenalin wird als Notfall-Arzneimittel in der Intensivmedizin (bei Erwachsenen in einer Dosierung von 2–16 µg/min)[10] verwendet. Es leistet gute Dienste bei der Behandlung von folgenden Krankheitsbildern:
- anaphylaktischer Schock
- Hypotonie
- kardiogener Schock
- septischer Schock
- Vergiftungen mit Vasodilatation
Es wird dabei intravenös meistens mittels Spritzenpumpe verabreicht. Noradrenalin soll so niedrig wie möglich dosiert werden, da es dem Herzen die Pumparbeit erschwert. Hauptzielparameter der Dosierung ist eine ausreichende Nierenausscheidung.
Kontraindikationen
Noradrenalin darf nicht oder nur sehr vorsichtig bei folgenden Zuständen angewandt werden:
- Bluthochdruck (arterielle Hypertonie)
- Cor pulmonale
- Engwinkelglaukom
- Hyperthyreose
- Phäochromozytom
- schwerer Arteriosklerose mit Stenosen
- schwerer Koronarsklerose oder schwerer Herzmuskelinsuffizienz
- schwerer Niereninsuffizienz
- Supraventrikuläre Tachykardie
- Tachyarrhythmie
- Vergrößerung der Prostata mit Restharnbildung
Handelsnamen
Monopräparate: Arterenol (D), sowie als Generikum (CH)
Kombinationspräparate: Scandonest (CH)
Literatur
- Hermann Voss, Robert Herrlinger (Begründer): Taschenbuch der Anatomie. Band 3: Nervensystem, Sinnessystem, Hautsystem, Inkretsystem. 17., überarbeitete Auflage. Fischer, Stuttgart 1986, ISBN 3-437-00487-5.
- Reinhard Larsen: Anästhesie und Intensivmedizin in Herz-, Thorax- und Gefäßchirurgie. (1. Auflage 1986) 5. Auflage. Springer, Berlin / Heidelberg / New York u. a. 1999, ISBN 3-540-65024-5, S. 44–46.
Weblinks
- Noradrenalinbestimmung im Urin. ( vom 23. September 2012 im Internet Archive) uni-duesseldorf.de
Einzelnachweise
- ↑ a b c Eintrag zu Noradrenalin. In: Römpp Online. Georg Thieme Verlag, abgerufen am 30. Mai 2014.
- ↑ a b Royal Pharmaceutical Society (Hrsg.): Clarke’s Analysis of Drugs and Poisons FOURTH EDITION. Pharmaceutical Press, London/Chicago 2011, ISBN 978-0-85369-711-4.
- ↑ a b Eintrag zu Norepinephrin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2020. (JavaScript erforderlich)
- ↑ H. Langecker, H. Friebel: Die Bedeutung der N-substitution bei der adrenergischen Ubertragung. In: Naunyn-Schmiedebergs Archiv Fur Experimentelle Pathologie Und Pharmakologie. 226. Jahrgang, Nr. 5, 1955, S. 493–504, PMID 13309387.
- ↑ Paul Martini: Über das Wesen und die Behandlung des essentiellen Hochdrucks. In: Münchener Medizinische Wochenschrift. Band 95, Nr. 1, 2. Januar 1953, S. 33–42 (O. Bollinger-Vorlesung, gehalten in München am 11. Dezember 1952), hier: S. 34.
- ↑ Paul Martini: Über das Wesen und die Behandlung des essentiellen Hochdrucks. In: Münchener Medizinische Wochenschrift. Band 95, Nr. 1, 2. Januar 1953, S. 33–42 (O. Bollinger-Vorlesung, gehalten in München am 11. Dezember 1952), hier: S. 34.
- ↑ Wolf-Dieter Müller-Jahncke, Christoph Friedrich, Ulrich Meyer: Arzneimittelgeschichte. 2., überarbeitete und erweiterte. Auflage. Wissenschaftliche Verlags-Gesellschaft, Stuttgart 2005, ISBN 978-3-8047-2113-5, S. 167.
- ↑ R.W. Fuller: Pharmacology of brain epinephrine neurons. In: Annu. Rev. Pharmacol. Toxicol. 22. Jahrgang, 1982, S. 31–55, PMID 6805416.
- ↑ Jassal/D’Eustachio/reactome.org: Dopamine is oxidised to noradrenaline
- ↑ Reinhard Larsen: Anästhesie und Intensivmedizin in Herz-, Thorax- und Gefäßchirurgie. (1. Auflage 1986) 5. Auflage. Springer, Berlin / Heidelberg / New York u. a. 1999, ISBN 3-540-65024-5, S. 44–46 und 76.
Auf dieser Seite verwendete Medien
Global harmonisiertes System zur Einstufung und Kennzeichnung von Chemikalien (GHS): Piktogramm für giftige / toxische Chemikalien
Struktur von Adrenalin
Struktur von Noradrenalin


