Nitroimidazole
In der Pharmakologie sind Nitroimidazole eine Stoffgruppe, die zur Behandlung von Infektionen mit Bakterien und/oder Protozoen dienen und deren Kernmerkmal ein mit einer Nitrogruppe substituiertes Imidazol ist. Imidazol ist eine fünfgliedrige heterocyclische organische Verbindung mit zwei Stickstoffatomen.
Medizinisch bedeutsam sind vor allem die Abkömmlinge des 5-Nitroimidazols („5-Nitromidazole“). Der wichtigste Vertreter ist das Metronidazol (Clont, Flagyl u. a.).
- 1-Nitroimidazol
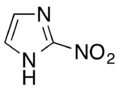
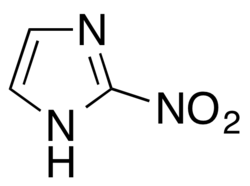
- 2-Nitroimidazol
- 5-Nitroimidazol
Die ebenfalls den Nitroimidazolen zuzurechnenden neueren Wirkstoffe Delamanid und Pretomanid werden in der Behandlung der Tuberkulose eingesetzt.
Entwicklung
Die Entwicklung der Nitroimidazole ging von dem 1953 aus einer Streptomyces-Art isolierten Azomycin (2-Nitroimidazol) aus, das sich als hochwirksam gegen Trichomonaden erwies, wegen seiner Toxizität aber nicht klinisch eingesetzt werden konnte.[1]
Der erste und wichtigste Vertreter der Nitroimidazole, Metronidazol, wurde 1960 von Rhône-Poulenc patentiert. Neuere Varianten wie Tinidazol (Simplotan, Sorquetan) und Nimorazol (Esclama) haben sich in Deutschland nicht dauerhaft auf dem Markt durchsetzen können.
Zu Beginn des 21. Jahrhunderts wurden mit Delamanid und Pretomanid zwei neue Nitroimidazolabkömmlinge[2] entwickelt, die gegen multiresistente Tuberkuloseerreger einsetzbar sind.[3] Delamanid wurde 2014 als Deltyba in der EU,[4] Pretomanid 2019 in den USA zugelassen.[5]
Vertreter
Die Tabelle enthält eine Übersicht über die wichtigsten Vertreter.
| Freiname | Systematischer Name | Einsatzgebiet | Resorption nach oraler Gabe | Halbwertszeit |
|---|---|---|---|---|
| 5-Nitroimidazole | ||||
| Metronidazol | 2-Methyl-5-nitroimidazol-1-ethanol | Humanmedizin | > 90 %[6] | 7 Std.[6] |
| Tinidazol | 1-[2-(2-Ethylsulfonyl)ethyl]-2-methyl-5-nitroimidazol | Humanmedizin | > 90 %[6] | 13 Std.[6] |
| Nimorazol | 4-[2-(5-Nitroimidazol-1-yl)ethyl]morpholin | Humanmedizin | hoch[6] | 10 Std.[6] |
| Ornidazol | (RS)-1-Chlor-3-(2-methyl-5-nitroimidazol-1-yl)propan-2-ol | Humanmedizin | 13 Std.[7] | |
| Fexinidazol | 1-Methyl-2-{[4-(methylthio)phenoxy]methyl}-5-nitro-1H-imidazol | Humanmedizin | 14 Std. (aktive Metaboliten: 15 Std. (M1) und 23 Std. (M2)[8]) | |
| Dimetridazol | 1,2-Dimethyl-5-nitroimidazol | Tiermedizin | ||
| Carnidazol | O-Methyl-N-[2-(2-methyl-5-nitroimidazol-1-yl)ethyl]carbamothioat | Tiermedizin | ||
| Ronidazol | 1-Methyl-2-[(carbamoyloxy)methyl]-5-nitroimidazol | Tiermedizin | ||
| 2-Nitroimidazole | ||||
| Benznidazol | N-Benzyl-2-nitroimidazol-1-ylacetamid | Humanmedizin | > 90 % | ca. 12 Std.[9] |
| Bicyclische Nitroimidazole | ||||
| Pretomanid | (6S)-2-nitro-6-{[4-(trifluormethoxy)benzyl]oxy}-6,7-dihydro-5H-imidazo[2,1-b][1,3]oxazin[10] | Humanmedizin | 16,0 bis 17,4 Std.[11] | |
| Delamanid | (2R)-2-Methyl-6-nitro-2-[(4-{4-[4-(trifluormethoxy)phenoxy]piperidin-1-yl}phenoxy)methyl]-2,3-dihydroimidazo[2,1-b]oxazol | Humanmedizin | hoch | 30–38 Std.[12] |

Wirkspektrum und Anwendungsgebiete
Das Wirkspektrum umfasst obligat anaerobe Bakterien (mit Ausnahme von Aktinomyzeten) und einige Protozoen (Entamoeba histolytica, Trichomonas vaginalis, Giardia lamblia). Aerobe und fakultativ anaerobe Bakterien (beispielsweise Propionibakterien) sind resistent.[6]
2- und 5-Nitroimidazole sind zur Behandlung von Infektionen wie Trichomoniasis, Aminkolpitis, Giardiasis, Amöbenruhr, Amöben-Leberabszess sowie diversen weiteren Anaerobierinfektionen (unter anderem mit Clostridium difficile) angezeigt.[13] Das Therapieschema (Einmalgabe oder Mehrfachgabe) hängt von der zugrundeliegenden Erkrankung ab. Mögliche Risiken einer längerfristigen Einnahme sind nicht erforscht. Benznidazol wird in der Humanmedizin in der Behandlung der akuten Phase der Chagas-Krankheit eingesetzt. Die Wirkstoffe sind oral verabreichbar.
In der Tiermedizin sind Dimetridazol (Chevi-col), Ronidazol (Ridzol) und Carnidazol (Spartrix) in Deutschland zur Behandlung der Trichomonadose bei Brieftauben zugelassen, können aber auch ggf. bei Klein- und Heimtieren eingesetzt werden. Die Anwendung bei lebensmittelliefernden Tieren ist verboten.
Delamanid und Pretomanid werden in der Humanmedizin, jeweils immer in Kombination mit weiteren Antituberkulotika, zur oralen Behandlung der multiresistenten Tuberkulose verwendet, wenn keine anderen Therapieoptionen bestehen.[4][5][14]
Pharmakodynamik
Die bakterizide Wirkung der 2- und 5-Nitroimidazole entfaltet sich intramikrobiell, wobei erst durch Reduktion der Nitrogruppe die hochwirksamen Metaboliten entstehen, welche intrazellulär die bakterielle DNA schädigen. Die Reduktion wird dabei erst durch anaeroben Stoffwechsel ermöglicht, was den Einsatz der Nitroimidazole gegen Anaerobier erklärt. Bei der DNA-Schädigung stehen vor allem Adduktbildungen mit benachbarten Basenpaaren eines DNA-Strangs im Vordergrund, die je nach Stärke der Bindungsstörung zu Strangbrüchen führen können.[13] Die Nitroimidazole haben dadurch einerseits einen bakteriziden Effekt, andererseits einen mutagenen (erbgutschädigenden) Effekt, wobei die Metaboliten allgemein eine höhere Affinität zu Bakterienzellen als zu menschlichen Zellen aufweisen, was überhaupt den Einsatz dieser mutagenen Substanzen in der Medizin ermöglicht.
Delamanid und Pretomanid sind Prodrugs. Für die Wirksamkeit muss zuvor in vivo – unter Beteiligung des Coenzyms F420 des Mycobacterium tuberculosis – eine aromatische Nitrogruppe durch Reduktion aktiviert werden.[5] Die entstandenen reaktiven Produkte hemmen die Mykolsäuresynthese von Mykobakterien.[14] Der Effekt ist bakterizid.
Kontraindikationen
Nitroimidazole dürfen nicht bei Erkrankungen des zentralen oder peripheren Nervensystems, Bluterkrankungen, Überempfindlichkeit und bei schweren Leberschäden angewendet werden. In der Schwangerschaft und Stillperiode bzw. Trächtigkeit sind sie wegen der potentiell teratogenen Wirkung nur bei strenger Indikationsstellung (lebensgefährliche Infektionen) zugelassen, da der Wirkstoff die Plazentaschranke überwindet.
Nitroimidazole führen durch Hemmung der Aldehyddehydrogenasen zu Intoleranz gegenüber Alkohol.[15] Bei gleichzeitigen Alkoholkonsum können schwere Nebenwirkungen und akute Intoxikationen (Vergiftungserscheinungen) eintreten. Hingegen bewirkt das Nitroimidazol Ornidazol (Tiberal) im Gegensatz zu anderen Vertretern der Gruppe keine Hemmung der Aldehyddehydrogenase und somit auch keine Alkoholunverträglichkeit.[7]
Nebenwirkungen
Häufige unerwünschte Nebenwirkungen der Nitroimidazole treten in Form von Magen-Darm-Beschwerden auf. Außerdem kann es zu Geschmacksstörungen kommen in Form eines metallischen Geschmacksempfindens.[16] Weitere Nebenwirkungen sind Kopfschmerz, Schwindel, Benommenheit, Parästhesien und allergische Reaktionen, selten auch Neuropathien, die nach Abbruch der Einnahme reversibel sein können.
Nitroimidazole wirken als Mutagene. Bei Mäusen weist Metronidazol eine karzinogene Wirkung auf, doch konnten ähnliche Studien bei Hamstern und große epidemiologische Studien an Menschen keinen Beweis für ein erhöhtes karzinogenes Risiko beim Menschen feststellen.
Einzelnachweise
- ↑ Eintrag zu Nitroimidazole. In: Römpp Online. Georg Thieme Verlag, abgerufen am 7. Juni 2014.
- ↑ B.M. Lee et al.: Predicting nitroimidazole antibiotic resistance mutations in Mycobacterium tuberculosis with protein engineering. In: PLoS Pathogens. Band 16 (2020), Nr. 2, doi:10.1371/journal.ppat.1008287.
- ↑ E. H. Ignatius, K. E. Dooley: New Drugs for the Treatment of Tuberculosis. In: Clinics in Chest Medicine. Band 40 (2019), S. 811–827, doi:10.1016/j.ccm.2019.08.001.
- ↑ a b D. Biermann: EU-Zulassung von Delamanid gegen multiresistente Tuberkulose, Pharmazeutische Zeitung, 14. Mai 2014.
- ↑ a b c A. Mende: US-Zulassung für neues Tuberkulosemittel, Pharmazeutische Zeitung, 15. August 2019.
- ↑ a b c d e f g E. Mutschler: Arzneimittelwirkungen. 7. Auflage, WVG, Stuttgart 1996, S. 692 ff.
- ↑ a b Fachinformation Tiberal (OrPha Swiss GmbH), Stand 2004.
- ↑ Fachinformation Fexinidazole Winthrop. Stand: 15. November 2018.
- ↑ Martindale. The Complete Drug Reference 38th Edition. London; Pharmaceutical Press; 2014. S. 929 f.
- ↑ Compounds | TB Alliance. Abgerufen am 7. Mai 2020.
- ↑ Pretomanid Tablets, Presciption Information (PDF), Stand August 2019.
- ↑ Alphienes Stanley Xavier, Mageshwaran Lakshmanan: Delamanid: A new armor in combating drug-resistant tuberculosis. In: Journal of Pharmacology & Pharmacotherapeutics. Band 5, Nr. 3, 2014, S. 222–224, doi:10.4103/0976-500X.136121, PMID 25210407, PMC 4156838 (freier Volltext).
- ↑ a b K. Aktories: Allgemeine und spezielle Pharmakologie und Toxikologie. 9. Auflage.
- ↑ a b G. Geisslinger et al.: Mutschler Arzneimittelwirkungen. 11. Auflage. WVG, Stuttgart 2019, S. 1048.
- ↑ E. Mutschler: Arzneimittelwirkungen. 9. Auflage. Wissenschaftliche Verlagsgesellschaft, Stuttgart 2008, ISBN 978-3-8047-1952-1.
- ↑ Sabine Cyrys: Viererband Grundlagenfächer. 2002, ISBN 3-437-42120-4, S. 427.
Auf dieser Seite verwendete Medien
Übersicht über die Struktur der Nitroimidazole