Bisphenol-A-diglycidylether
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||||||
| Struktur ohne Darstellung der Stereochemie | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Bisphenol-A-diglycidylether | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C21H24O4 | |||||||||||||||||||||
| Kurzbeschreibung | farblose, geruchlose Flüssigkeit[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 340,41 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand | zähflüssig | |||||||||||||||||||||
| Dichte | 1,16 g·cm−3[1] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Dampfdruck | vernachlässigbar[1] | |||||||||||||||||||||
| Löslichkeit | praktisch unlöslich in Wasser (0,7 mg·l−1 bei 25 °C)[1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Bisphenol-A-diglycidylether (abgekürzt BADGE oder DGEBA nach Diglycidylether von Bisphenol A) ist eine chemische Verbindung, die als Monomer zur Herstellung von Epoxidharzen und Phenolharzen genutzt wird. Es ist ein Derivat von Bisphenol A, das auf Grund seiner Fähigkeit zur Vernetzung ebenfalls zur Herstellung von Epoxidharzen genutzt wird.[3]
Synthese
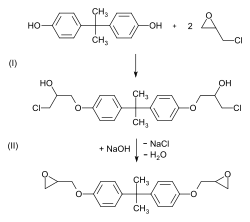
Bisphenol-A-diglycidylether wird aus Bisphenol A mit einem Überschuss an Epichlorhydrin hergestellt. In einer zweistufigen Reaktion wird zunächst Epichlorhydrin an Bisphenol A addiert und daraus anschließend mit einer stöchiometrischen Menge Natronlauge das Bis-Epoxid gebildet.

Chemische Eigenschaften
Stereochemie
Bisphenol-A-diglycidylether liegt in der Regel als Stereoisomerengemisch vor.
- (R,S)-Isomer
- (R,R)-Isomer
- (S,S)-Isomer
Die (R,R)-Form bildet dabei mit der (S,S)-Form ein Racemat, bei der (R,S)-Form handelt es sich um eine achirale meso-Form. Im Gemisch liegen alle drei stereoisomeren Formen vor.
Verwendung
Der Aufbau vieler Standard-Epoxide basiert auf Diglycidylethern, darunter auch BADGE.[4] Epoxidharze sind empfindlich gegen hohe Temperaturen, Säurespuren und addieren leicht Thiole sowie Amine. Die häufigsten Härter für Epoxidharze sind Polyamine, Aminoamide und phenolische Verbindungen.[5]
Beschichtungen auf der Basis von BADGE-enthaltenden Epoxidharzen werden zur Innenauskleidung von Konservendosen und Schraubverschlüssen (Twist-off-Deckel) benutzt. BADGE könnte aus diesen Beschichtungen als unreagiertes Monomer in Lebensmittel übertreten.[6]
Sicherheitshinweise
BADGE ist als eine Gruppe-3-Chemikalie der Internationale Agentur für Krebsforschung (IARC) gelistet, was bedeutet, dass es „nicht klassifizierbar hinsichtlich seiner Karzinogenität für den Menschen“ ist.[7][8] Seit den 1990ern kamen Bedenken hinsichtlich der Karzinogenität auf, vor allem weil BADGE wie erwähnt mit Nahrungsmittel in Kontakt tritt.[3]
In Meeressäugern wurden ähnliche bis höhere Konzentrationen des chlorierten Vorläuferprodukts von BADGE gefunden als von persistenten organischen Schadstoffen wie polybromierten Diphenylethern oder Perfluoroctansulfonat.[9]
Bisphenol-A-diglycidylether wurde 2013 von der EU gemäß der Verordnung (EG) Nr. 1907/2006 (REACH) im Rahmen der Stoffbewertung in den fortlaufenden Aktionsplan der Gemeinschaft (CoRAP) aufgenommen. Hierbei werden die Auswirkungen des Stoffs auf die menschliche Gesundheit bzw. die Umwelt neu bewertet und ggf. Folgemaßnahmen eingeleitet. Ursächlich für die Aufnahme von Bisphenol-A-diglycidylether waren die Besorgnisse bezüglich Verbraucherverwendung, hoher (aggregierter) Tonnage und weit verbreiteter Verwendung sowie der Gefahren ausgehend von einer möglichen Zuordnung zur Gruppe der CMR-Stoffe und als potentieller endokriner Disruptor. Die Neubewertung fand ab 2015 statt und wurde von Dänemark durchgeführt. Anschließend wurde ein Abschlussbericht veröffentlicht.[10][11]
Siehe auch
Weblinks
Einzelnachweise
- ↑ a b c d e f g Eintrag zu 2,2-Bis(4-(glycidyloxy)phenyl)propan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Februar 2016. (JavaScript erforderlich)
- ↑ Eintrag zu 2,2′-[(1-methylethylidene)bis(4,1-phenyleneoxymethylene)]bisoxirane im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. August 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ a b Walfried Rauter, Gerald Dickinger, Rudolf Zihlarz, Josef Lintschinger: Determination of Bisphenol A diglycidyl ether (BADGE) and its hydrolysis products in canned oily foods from the Austrian market. In: Zeitschrift für Lebensmitteluntersuchung und -Forschung A. 208. Jahrgang, Nr. 3, März 1999, S. 208–211, doi:10.1007/s002170050404.
- ↑ Umweltbundesamt:Empfehlung: Leitlinie zur hygienischen Beurteilung von organischen Beschichtungen im Kontakt mit Trinkwasser (Beschichtungsleitlinie). ( vom 26. April 2014 im Internet Archive) (PDF; 241 kB) vom 30. November 2010. Auf Umweltbundesamt.de, abgerufen am 16. Oktober 2024.
- ↑ Martin Forrest: Coatings and Inks for Food Contact Materials (= RAPRA review reports. Vol. 16, Nr. 6). iSmithers Rapra Publishing, 2005, ISBN 978-1-84735-079-4, S. 8.
- ↑ Bundesamt für Verbraucherschutz und Lebensmittelsicherheit (BVL), Hrsg., Amtliche Sammlung von Untersuchungsverfahren nach § 35 LMBG, Beuth: Berlin, (Loseblattsammlung); L 00.00-51; Methodensammlung BVL Online, Stand: 9. Dezember 2007.
- ↑ List of Classifications – IARC Monographs on the Identification of Carcinogenic Hazards to Humans. IARC, abgerufen am 14. Juli 2020.
- ↑ IARC Working Group on the Evaluation of Carcinogenic Risks to Humans (Hrsg.): Re-evaluation of some organic chemicals, hydrazine and hydrogen peroxide (= IARC monographs on the evaluation of carcinogenic risks to humans. Band 71). World Health Organization, International Agency for Research on Cancer, Lyon 1999, ISBN 978-92-832-1271-3, S. 1285–1289 (iarc.fr).
- ↑ Jingchuan Xue, Kurunthachalam Kannan: Novel Finding of Widespread Occurrence and Accumulation of Bisphenol A Diglycidyl Ethers (BADGEs) and Novolac Glycidyl Ethers (NOGEs) in Marine Mammals from the United States Coastal Waters. In: Environmental Science & Technology. 2016, doi:10.1021/acs.est.5b04650.
- ↑ Europäische Chemikalienagentur (ECHA): Substance Evaluation Conclusion and Evaluation Report.
- ↑ Community Rolling Action Plan (CoRAP) der Europäischen Chemikalienagentur (ECHA): 2,2'-[(1-methylethylidene)bis(4,1-phenyleneoxymethylene)]bisoxirane, abgerufen am 6. März 2022.
Auf dieser Seite verwendete Medien
Structure of (2R,2'R)-2,2'-(((propane-2,2-diylbis(4,1-phenylene))bis(oxy))bis(methylene))bis(oxirane)
Structure of (2R,2'S)-2,2'-(((propane-2,2-diylbis(4,1-phenylene))bis(oxy))bis(methylene))bis(oxirane)
Structure of 2,2'-(((propane-2,2-diylbis(4,1-phenylene))bis(oxy))bis(methylene))bis(oxirane)
Structure of (2S,2'S)-2,2'-(((propane-2,2-diylbis(4,1-phenylene))bis(oxy))bis(methylene))bis(oxirane)
Autor/Urheber: Roland.chem, Lizenz: CC0
Synthese Diglycidether auf der Basis von Bisphenol A